首页产品注册/报批 > 进口药品注册 > 详情
流程指南
发布时间:2012/2/24阅读:815
进口医疗器械注册常见问题
法规依据
《药品注册管理办法》第一百零一条申请进口药品注册的,应当填写《药品注册申请表》,报送有关资料和样品,提供相关证明文件,向国家食品药品监督管理局提出申请。
《药品注册管理办法》第一百零二条 国家食品药品监督管理局对申报资料进行形式审查,认为符合要求的,予以受理,出具药品注册申请受理通知书,并通知中国药品生物制品检定所组织对3个生产批号的样品进行注册检验;认为不符合要求的,不予受理,出具药品注册申请不予受理通知书,并说明理由。
国家食品药品监督管理局根据需要,可以组织对研制情况及生产条件进行现场核查,并抽取样品。
《药品注册管理办法》第一百零三条 中国药品生物制品检定所完成进口药品注册检验后,应当将复核的药品标准、药品注册检验报告和复核意见报送国家食品药品监督管理局。
《药品注册管理办法》第一百零四条 国家食品药品监督管理局对申报资料进行全面审评,必要时可以要求申请人补充资料。认为需要进行临床试验的,发给《药物临床试验批件》;认为不符合规定的,发给《审批意见通知件》,并说明理由。
《药品注册管理办法》第一百零五条 临床试验获得批准后,申请人应当按照本办法第四章及有关要求进行试验。
临床试验结束后,申请人应当填写《药品注册申请表》,按照规定报送临床试验资料、样品及其他变更和补充的资料,并详细说明依据和理由,提供相关证明文件。
《药品注册管理办法》第一百零六条 国家食品药品监督管理局组织对报送的临床试验等资料进行全面审评,必要时可以要求申请人补充资料。认为符合规定的,发给《进口药品注册证》;中国香港、澳门和台湾地区的制药厂商申请注册的药品,参照进口药品注册申请的程序办理,认为符合要求的,发给《医药产品注册证》。认为不符合要求的,发给《审批意见通知件》,并说明理由。
《药品注册管理办法》第一百零七条 申请进口药品制剂,必须提供直接接触药品的包装材料和容器合法来源的证明文件、用于生产该制剂的原料药和辅料合法来源的证明文件。原料药和辅料尚未取得国家食品药品监督管理局的批准的,应当报送有关生产工艺、质量指标和检验方法等的研究资料。
《药品注册管理办法》第一百零八条 国家食品药品监督管理局在批准进口药品的同时,发布经核准的进口药品注册标准和说明书。
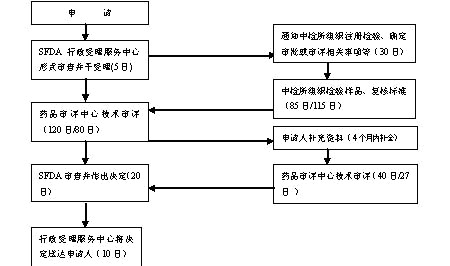
申报流程示意图: